前言
2025年9月25日,美国国立卫生研究院(NIH)发布重磅消息,宣布成立美国第一个标准化类器官建模中心(SOM),为期三年投入8700万美元,目标是创建一个开发、共享和验证类器官的新方法学平台。

9月25日,NIH宣布成立类器官建模中心SOM
该公告紧承此前NIH及美国食品药品监管局(FDA)一系列推动类器官作为动物替代模型的举措,再次着重强调了美国方面加注类器官平台的决心:
4月10日
FDA:计划逐步取消单克隆抗体及其他药物的动物实验要求,推动新方法论如类器官等的替代
4月29日
NIH:设立特别办公室ORIVA,推动“类器官优先 + 动物实验精准化”新模式
7月07日
NIH&FDA:不再资助仅依赖动物试验的新研究项目,所有新的NIH资助机会都应纳入新方法(NAMs)的考量
近两年来,类器官正从一种实验室概念模型加速迈向主流科学的中心。这种具有三维结构的微型器官能够在体外模拟人类组织的形态和部分功能,与传统动物模型相比,在遗传背景、免疫状态和代谢水平上更贴近人类,但长期以来始终停留在小规模、定制化阶段,继续政策与投资扶持。而与近来密集出台的监管与资助政策相呼应的是,近半年内,业内顶刊如Science、Nature、Cell等多次刊发类器官领域重磅突破,从血管化方案到多模型构建,正从“结构模仿”向“功能还原”大步飞跃。
事实上,回顾2024年底,类器官技术已经频频进入公众与学术的双重视野,不仅先后入选中国工程院与中国科学院分别发布的《全球工程前沿2024》及《2024研究前沿》,还在国际学界的视觉呈现中留下身影——来自基因组调控中心(CRG)的研究者Natalia Pardo Lorente 拍摄的类器官染色图被Nature评为年度最佳科学图片之一。这些信号意味着类器官正在从“实验室前沿”走向“全球共识”。在这样的背景下,进入2025年后,无论是监管层面的政策突破,还是顶刊不断刷新的模型与技术成果,都预示着这一领域将在今年迎来更密集的累积与更高层次的飞跃。

医药卫生领域遴选结果[1]
01 从动物试验向人源模型的转型升级
数十年来,动物模型一直是药物研发早期验证的基石。研究人员通常先在大鼠和小鼠中评估候选化合物的安全性与有效性,理由是其生理系统在一定程度上与人类相似。在更复杂或长期的研究中,狗及恒河猴等非人灵长类也被频繁使用。围绕这些实验对象甚至形成了庞大的产业链,据多方估算,全球动物实验及相关生物技术市场的体量已达到数百亿美元级别。
然而,这一体系始终伴随着局限与争议。动物试验成本高昂、饲养环境复杂,还持续引发伦理关注——动物权益组织正是近年来支持FDA改革的最积极群体之一。更为关键的是,动物模型并非理想的人体替代方案。统计数据显示,近九成候选药物在进入临床阶段后仍以失败告终。其背后的根本原因在于,物种间存在不可忽视的生理差异:某种分子或许能在小鼠模型中改善帕金森症状,但这并不意味着它同样能够在真实患者中发挥疗效。
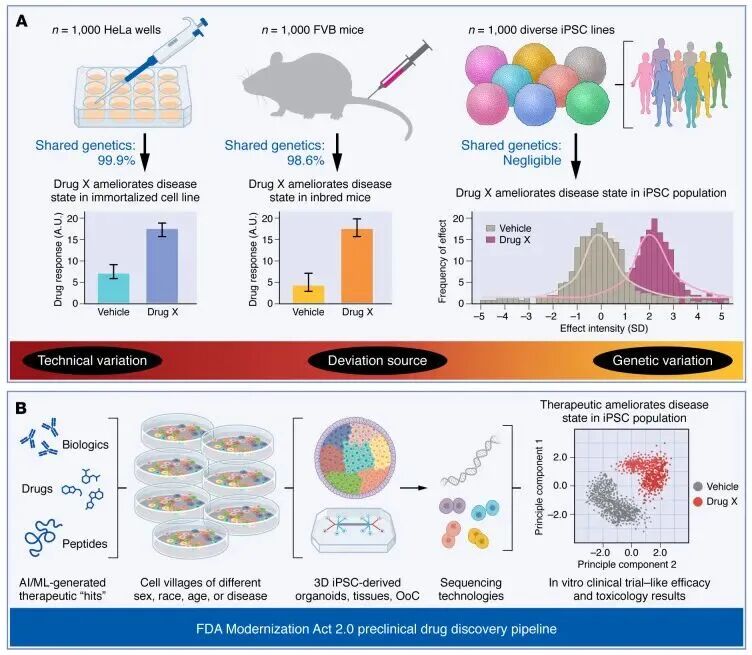
动物模型缺乏基因多样性且与人类间存在表型差异[2]
类器官技术通过干细胞三维自组装方法再现组织微结构,并在一定程度上模拟“疾病—反应—调控”链条。相对于动物模型,类器官技术体现出了显著的成本优势。与此同时,类器官的高通量筛选能力使研究人员能够同时测试数百种化合物,大幅提高研发效率。
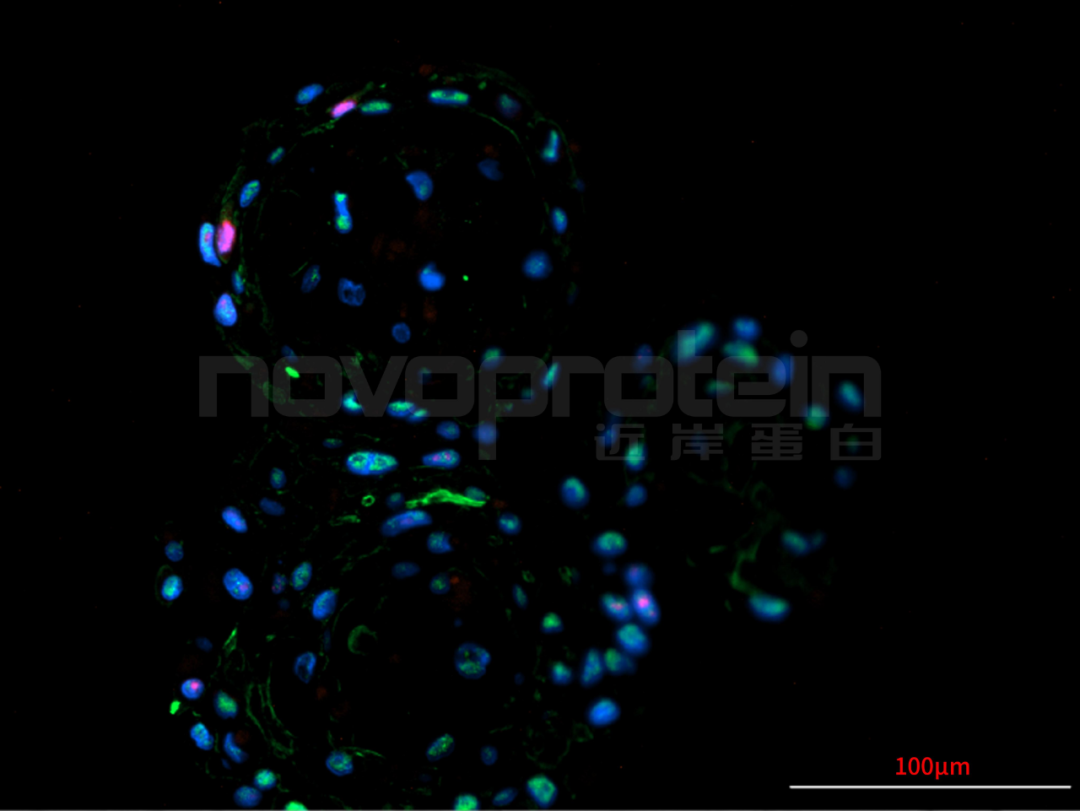
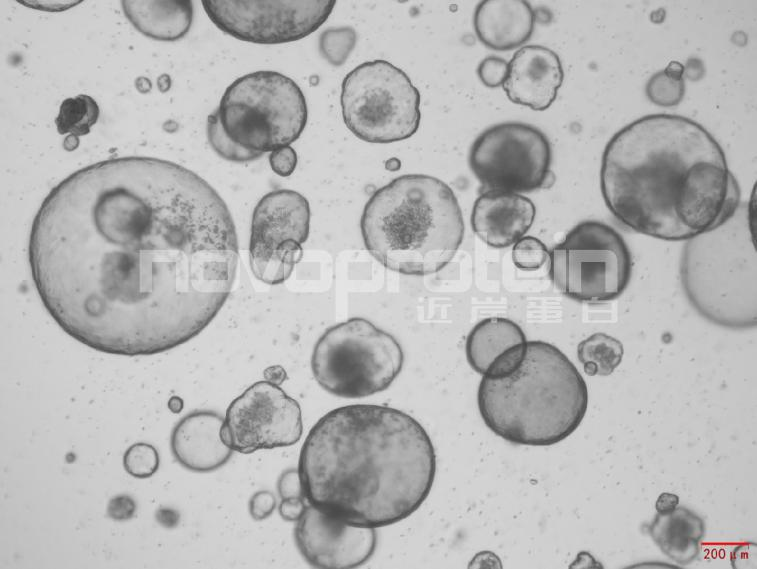
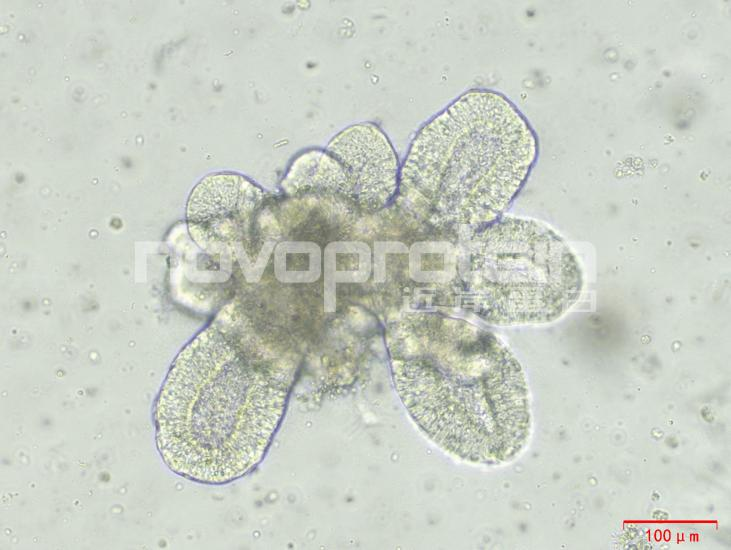
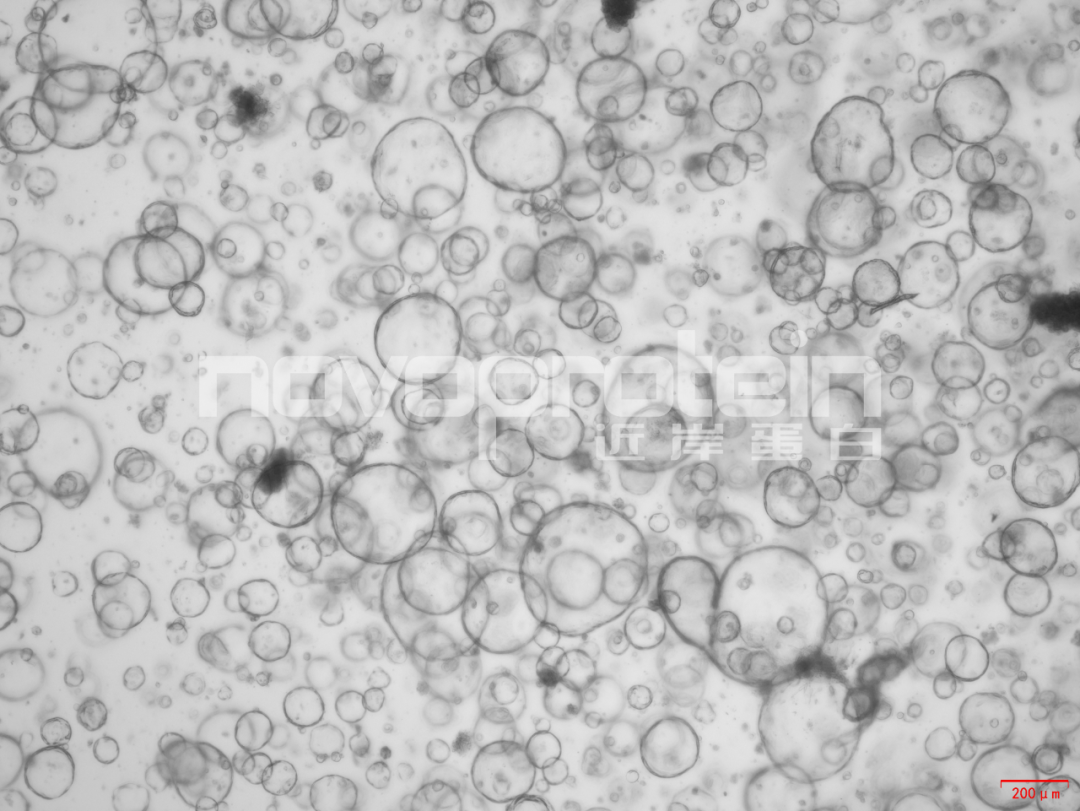
图:经近岸蛋白细胞因子验证培养的类器官(从左至右,从上至下:乳腺癌类器官、ipsc来源的人小肠类器官、小鼠胃类器官及小鼠胆管类器官)
02 政策动向:大力推动动物替代,人源模型提升体外模拟保真度
有鉴于动物试验的种种短板,自2022年起,FDA已经发布了现代化法案2.0,大力推动非动物试验新替代方法(NAMs)的普及,并将类器官及器官芯片视作一种重要的新替代方法模型。4月10日,FDA再次宣布改革计划,拟逐步撤销单克隆抗体等药物研发过程中的刚性动物测试要求,建议开发者采用人工智能建模、器官芯片和类器官等新方法来评估安全性与毒性。FDA 的公告指出,先进的计算模型和人源细胞模型不仅更具预测性,还能缩短研发周期、降低成本,并提高患者安全性。这一举动意味着,美国药品审评将首次正式接受非动物数据作为关键依据,为替代模型打开了一条法规之路。

4月10日,FDA宣布取消动物试验要求并同时发布一份《减少临床前安全性研究中动物实验的路线图》
与FDA的倡议相呼应,NIH在4月29日发布通告,宣布将优先支持基于人类生物学的研究技术,计划设立“研究创新、验证与应用办公室”(ORIVA)。据悉,ORIVA的核心目标是扩大对类器官、器官芯片、计算建模及真实世界数据等非动物技术的资助与培训,提升这些方法的转化效率,并逐步替代动物实验。通告强调,传统动物模型在转化医学中的局限性越来越明显,未来的资助评审将更看重实验模型与研究问题的匹配度,强调人相关性、情境适配和可转化性。为此,NIH要求评审过程中减少对动物研究的惯性偏好,并定期公布动物研究与人本研究经费分配比例。这一政策不仅从资金上鼓励研究者转向类器官等人相关模型,也通过透明化机制倒逼学界审视实验设计的合理性。

4月29日,NIH设立ORIVA
更加直接的信号出现在7月。多家媒体报道,NIH的新资助通知(NOFO)将不再针对“纯动物模型”设立专门资助,所有申请必须包含人体相关的新方法组件。美国毒理学替代研究中心副主任Nicole Kleinstreuer在接受采访时指出,这一决定将迫使研究者思考如何在早期就应用类器官、器官芯片或计算模型,以筛除无效方向;同时也意味着过去仅凭动物数据晋级临床的路线将逐渐收紧。

7月7日,NIH与FDA联合宣布不再资助仅依赖动物试验的新研究项目,所有新的NIH资助机会都应纳入新方法(NAMs)的考量
本次NIH宣布成立标准化类器官建模中心(SOM),宣布将利用人工智能、机器人和多来源人类细胞,系统优化培养流程,减少实验室之间的差异。中心承诺按照开放科学原则公布所有协议和数据,建设数字化资源库,为研究者提供经过验证的细胞材料和表征数据,并与FDA等监管机构合作,制定可直接用于审评的标准格式。可以说,SOM的设立标志着类器官从散点创新走向系统化、标准化阶段,这与ORIVA和FDA 的政策构成互相支撑的生态。
本次NIH公告首图为脑类器官成像
据称,SOM中心的核心是以下各项的强大组合:
-
人工智能(AI)和机器学习(ML)挖掘科学文献和实验数据以实时优化协议。
-
先进的机器人和成像技术以扩大类器官的生产规模,目标为每天分析超过100,000个样本。
-
通过异质性人类细胞来源确保类器官反映现实世界的生物学差异,包括年龄、性别和遗传祖先。
-
开放存取数字和物理存储库,以便科学家可以随时随地访问标准化协议、数据和活体类器官。
该中心最初将专注于肝脏、肺、心脏和肠道的类器官模型,并计划扩展到大脑、胸腺和其他特定疾病的模型。
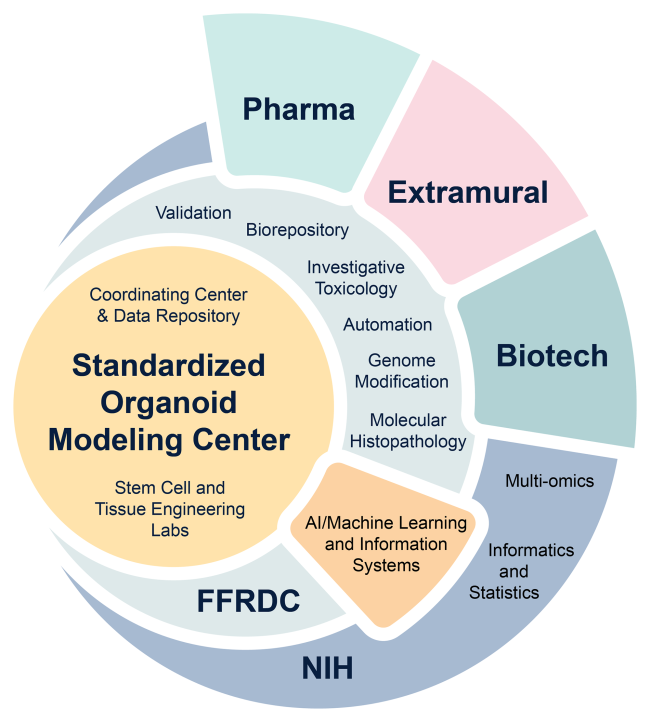
SOM中心将NIH的资源与其他联邦机构和行业合作伙伴联系起来,以促进合作并加速NAM技术的发展,造福更广泛的科学界。
总体而言,从 FDA 的监管转变到NIH的资助策略,再到 SOM 的基础设施投入,美国联邦层面已开始通过法规和资金双重杠杆把科学界引向“以人相关模型,尤其是类器官为中心”的新常态。这种趋势不仅会减少动物试验数量,更重要的是倒逼实验设计升级,让研究更聚焦于人体生物学与临床需求之间的真实联系。
03 科研突破:从结构模仿迈向功能还原
政策的“指挥棒”会显著改变研究风向,但技术的突破则决定了替代路径的可行性。根据PubMed,2025年至今,Nature接连发表类器官相关论文共计20篇,涉及多区域脑、肝脏、神经通路新模型,以及利用类器官进行的个性化ASO筛选、结直肠癌可塑性研究等工具性质的研究应用。Science和Cell相关文章则分别为9篇和5篇。总数量远高于去年同期(分别为16篇、3篇及9篇)。
2025年中,血管化和多谱系整合成为类器官科研的关键词。长期以来,由于缺乏血管供应,类器官的中心区域会出现营养和氧气缺乏,导致坏死,限制了模型的体积和成熟度。近期,该领域迎来集中突破式进展。MIT、哈佛与辛辛那提儿童医院的团队在Cell上联手提出内胚层与中胚层共发育方案[3]。他们从人多能干细胞出发,同时诱导内胚层形成肺或肠上皮,诱导中胚层生成内皮细胞和血管平滑肌细胞,并通过调整BMP和WNT信号时序,以及加入VEGF、ANG1等因子,成功在类器官内部构建了组织特异的血管网络。新生成的血管化肺类器官不仅具备肺泡样结构,还展现出与胎儿肺部相似的血管分支,细胞存活率显著提高。研究者指出,这些模型可用于研究罕见的肺毛细血管发育异常,更有助于气体交换相关的深入探索。
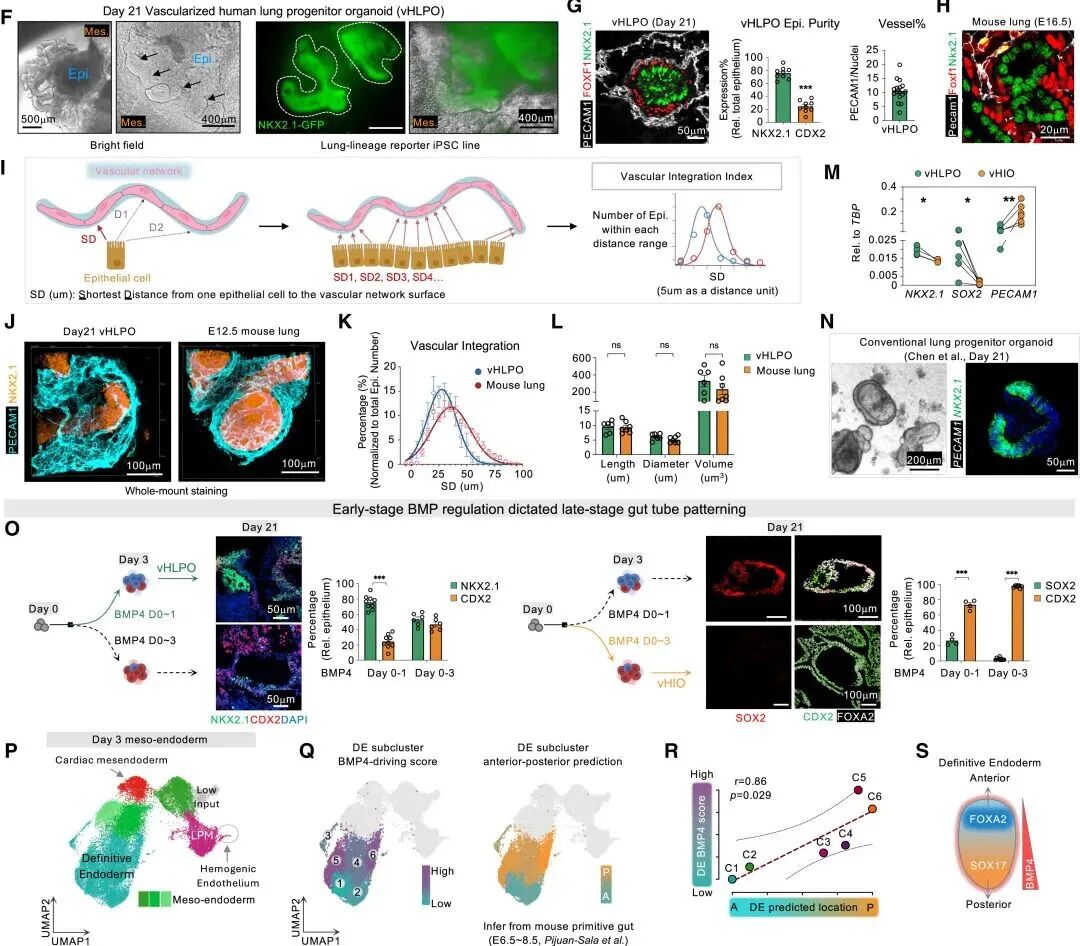
血管化肺/肠类器官的生成
同在6月,斯坦福大学团队在Science发文,将图案化微结构与分时信号组合应用于心脏和肝脏类器官的血管化[4]。他们设置了34种不同的生长因子组合,精确控制心肌细胞、内皮细胞和平滑肌细胞的比例与发育顺序。实验结果显示,在最佳条件下,类器官内部形成了完整的分支血管,并能与心肌电活动同步跳动,模拟孕6.5周胚胎心脏。值得注意的是,这一策略也可平移至肝脏类器官,打破了传统模型“单器官单方案”的限制,并为未来的再生医学和器官移植奠定技术基础。
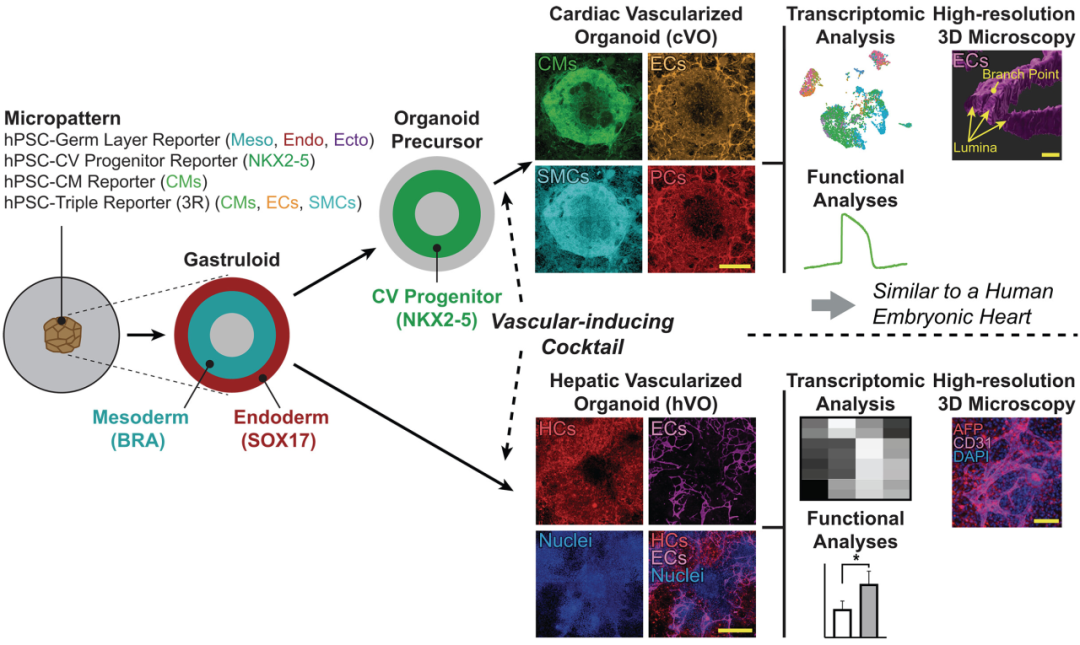
微模式化和生长因子的添加实现了类原肠胚、心血管、祖细胞和cVO的体外形成
另一个引人关注的创新来自哈佛医学院和北京大学的合作[5]。研究者采用所谓“正交转录激活”策略,在中胚层祖细胞中同步激活转录因子ETV2和NKX3.1,在五天内快速生成血管类器官(VOs)。这些VO在体外表现出正确的顶底极性和早期管腔结构,嵌入基质胶后,血管网络迅速扩张并呈现动脉化趋势;移植到小鼠肾包膜和后肢缺血模型中后,VOs能稳定灌注并重建血管网络,提高局部血流和组织修复效果。该成果说明,通过调控关键基因网络可以极大缩短类器官建模时间,为再生医学提供更高效的平台。
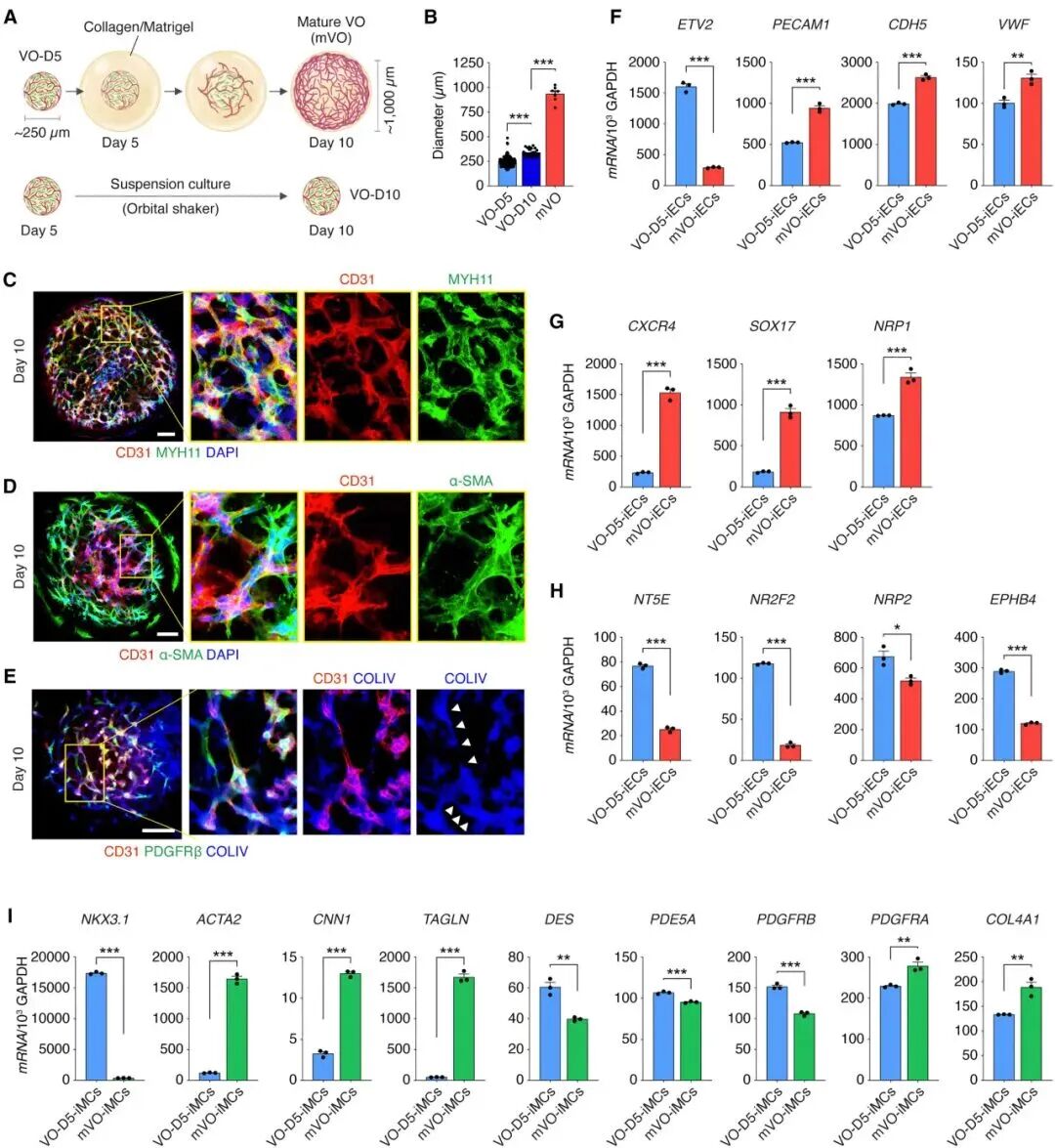
嵌入基质胶有助于VO的成熟
在脑科学领域,约翰·霍普金斯大学团队构建的全脑类器官(MRBO)让神经系统模型从单一脑区走向多区域协同[6]。研究者分别培养大脑皮层、中脑/后脑和内皮类器官,再利用基质材料把它们融合在一起,使不同脑区的神经元及血管细胞保持身份并形成功能连接。MRBO展现了约80%的早期脑细胞类型,比传统皮层类器官更加复杂。更重要的是,融合模型中出现了初步的血脑屏障迹象,说明内皮与神经系统可以在体外共发育。该团队指出,基于动物的神经系统模型往往无法反映人类脑部的区域互作和血脑屏障特性,而MRBO为研究精神疾病、药物穿透以及个体化神经治疗提供了全新的平台。
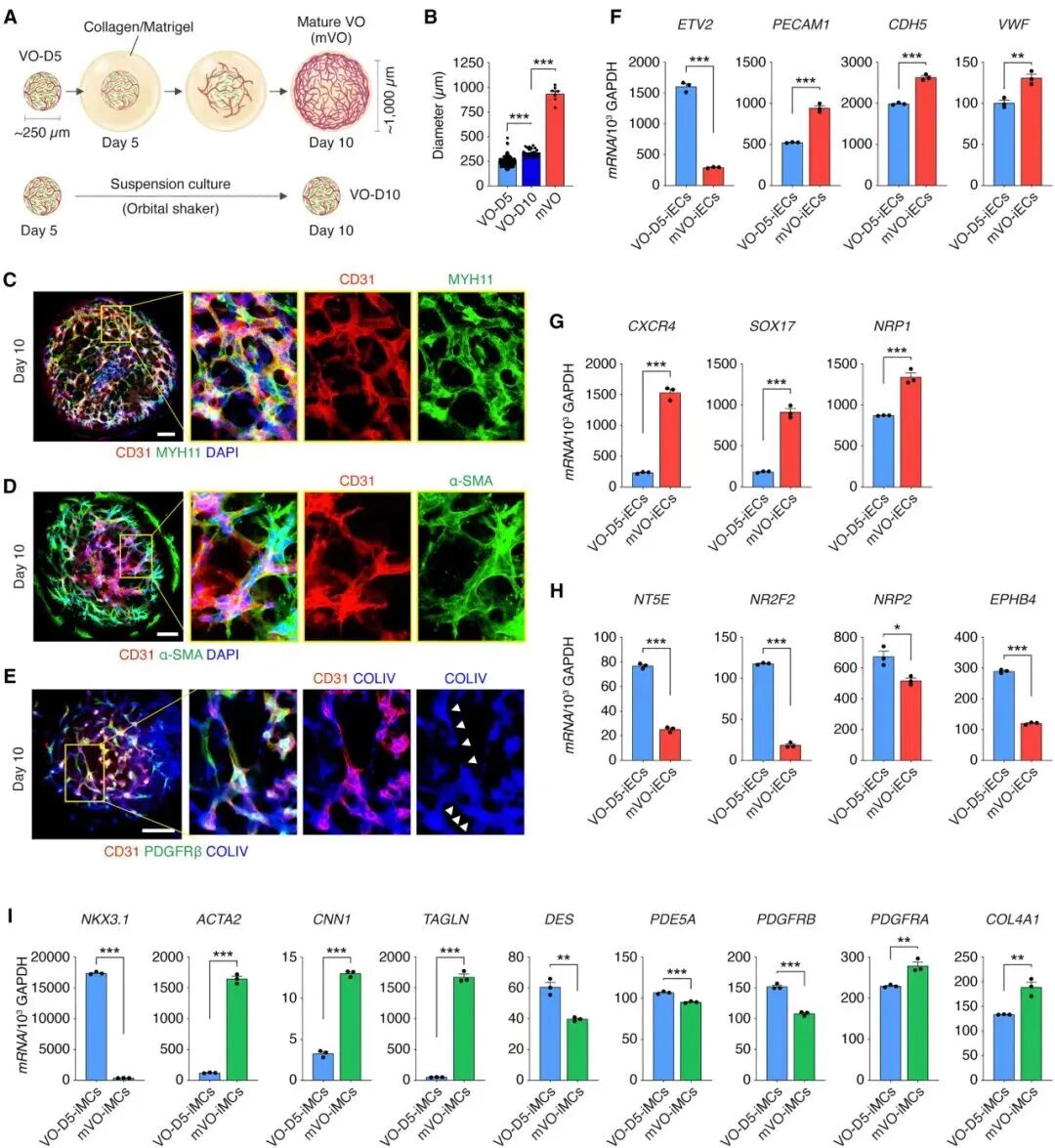
图:MRBOs的生成和分子表征
总而言之,所有突破共同指向一个趋势:类器官正在从单一细胞层面的结构模拟迈向多细胞、多系统的功能还原。血管化和神经-血管互作的实现,显著提升了模型的成熟度和可用时间窗口,使其不再只是“微缩的器官影子”,而是真正的微型生理系统。随着政策鼓励和平台化设施的推出,越来越多的团队将能够在标准化基础上迭代方案,加速科学和临床应用。
04 产业动能:快速增长的市场与协同生态
政策推动和科研突破迅速引爆了产业界的热情。根据 Research and Markets2025年4月发布的市场报告,全球人类类器官市场从2024年的11.1亿美元增长到2025 年的12.6亿美元,预计到2030年将达到25.8亿美元,年复合增长率约15%。报告指出,这一增长得益于先进培养技术的扩散和监管政策的利好,同时也反映出制药公司、科研机构及投融资机构对该领域的信心。
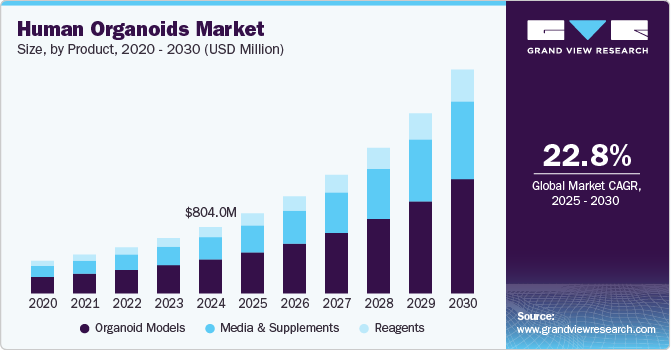
类器官市场规模走势[7]
与此同时,行业竞争者的版图也在迅速扩张。2024年年底,默克集团美国与加拿大生命科学业务部门MilliporeSigma宣布收购“类器官之父”公司HUB Organoids Holding B. V.。HUB首席执行官Robert Vries表示,HUB的专利技术处在推动药物发现和研发范式转型升级的最前沿,而默克的资源将成为HUB业务的助推器,促使HUB更积极地拓宽业务版图并扩大在客户及患者间的影响力。此外,类器官芯片开发商Emulate已与mRNA疫苗头部企业Moderna合作,使用器官芯片筛选mRNA递送载体脂质纳米颗粒的安全性。器官芯片制造商Hesperos已与赛诺菲、阿斯利康、Argenx和Apellis Pharmaceuticals合作,筛选候选药物在神经退行性疾病和其他疾病中的安全性和有效性。Samsung Biologics 则在2025年6月宣布推出 “Samsung Organoids”服务(即将类器官纳入其药物研发服务组合),标志大型CDMO/生物制造公司开始把类器官作为其技术栈的一环。
根据 Towards Healthcare发布的《iPSC平台市场规模与趋势预测》报告,在基于iPSC的平台市场中,类器官和3D培养平台预计将在未来几年呈现最高增长。随着3D生物打印、磁悬浮和高内涵成像等技术的成熟,研究人员可以更精细地调整类器官的空间结构和微环境,延长其存活时间并提高功能表达。合作方面,学术机构、医疗机构和企业的协同成为常态,实时临床反馈被纳入研发流程,加快了从试验台到临床应用的转换。资本方面,既有风险投资也有制药巨头参与布局,他们看中的不仅是当前的市场空间,更是类器官在精准医学和新药开发中的战略价值。政策上,FDA表示愿意将经验证的类器官数据纳入IND申请渠道,并通过监管激励支持行业创新。这一系列因素共同推动产业从“探索期”进入“扩张期”,类器官正在被视为下一个具备颠覆性潜力的生物医学平台。
04 迈向以人类为中心的生物医学时代
综合看来,传统动物模型的可靠性与效率已难以满足精准医疗的需求,人相关的类器官和相关新方法正在从“备选方案”转变为“第一标准”。FDA的新规打破了动物试验的制度束缚,NIH通过调整资助导向和建立 ORIVA为非动物研究提供了资源保障,SOM中心则为标准化和验证提供了技术支撑fda.gov。与此同时,血管化、多区域融合以及快速培养等科研进展使类器官的功能接近真正的器官,市场规模和企业布局也显示出商业化的巨大潜力。
当然,新的模型替代并不会在一夜之间全面完成。未来一段时间内,动物实验仍在某些领域扮演不可替代的角色。但随着标准体系的逐渐完善、伦理框架的制定以及跨学科技术的成熟,类器官无疑将在新药筛选、疾病建模、精准治疗和再生医学中承担越来越核心的任务。在即将到来的以“人相关性”为核心的生物医学时代,这些微小而复杂的模型将成为连接基础研究与临床应用的桥梁,帮助我们更快、更安全地破解人类疾病的谜团。
近岸蛋白相关产品
近岸蛋白依靠专业的研发团队,精心打造类器官验证平台,可提供一系列经验证、高活性、高稳定性的类器官培养产品,助您高效快速开展类器官实验!
NovoMatrix-经类器官培养验证的基质胶
近岸蛋白提供经类器官/干细胞培养验证的系列NovoMatrix基质胶,产品批次稳定可控,让您的类器官/干细胞培养更可控!
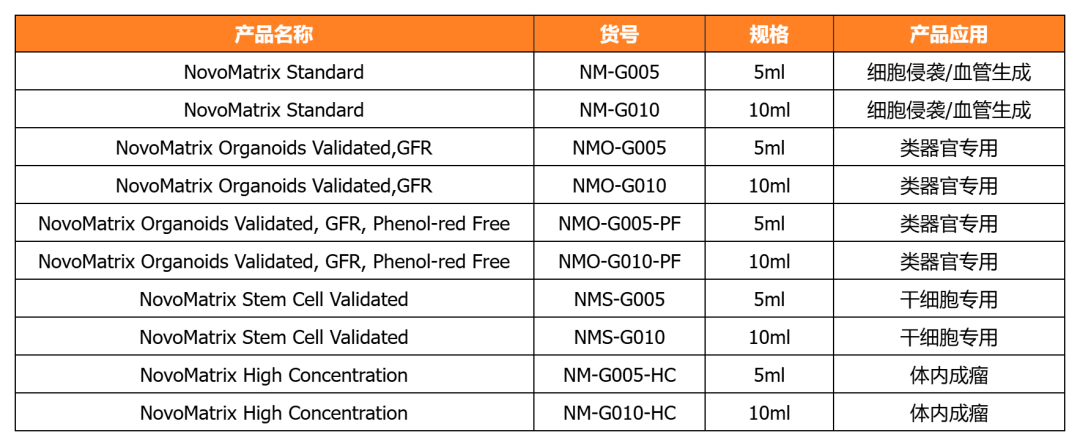
NovoMatrix支持多种类器官培养
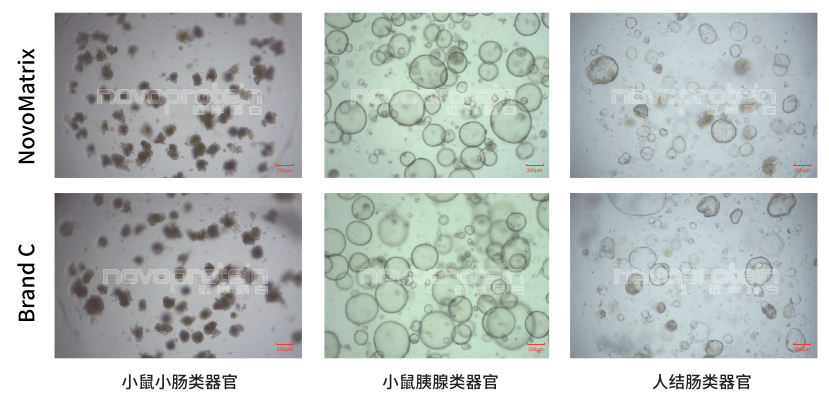
NovoMatrix Organoid Validated,GFR,Phenol Red-Free (Cat.No.:NMO-G005-PF) and a similar product of Brand C were used for culture of different oragnoid models
NovoMatrix支持类器官稳定传代

NovoMatrix Organoid Validated,GFR,Phenol Red-Free (Cat.No.:NMO-G005-PF) maintain stable passage of organoids comparable to a similar product of Brand C
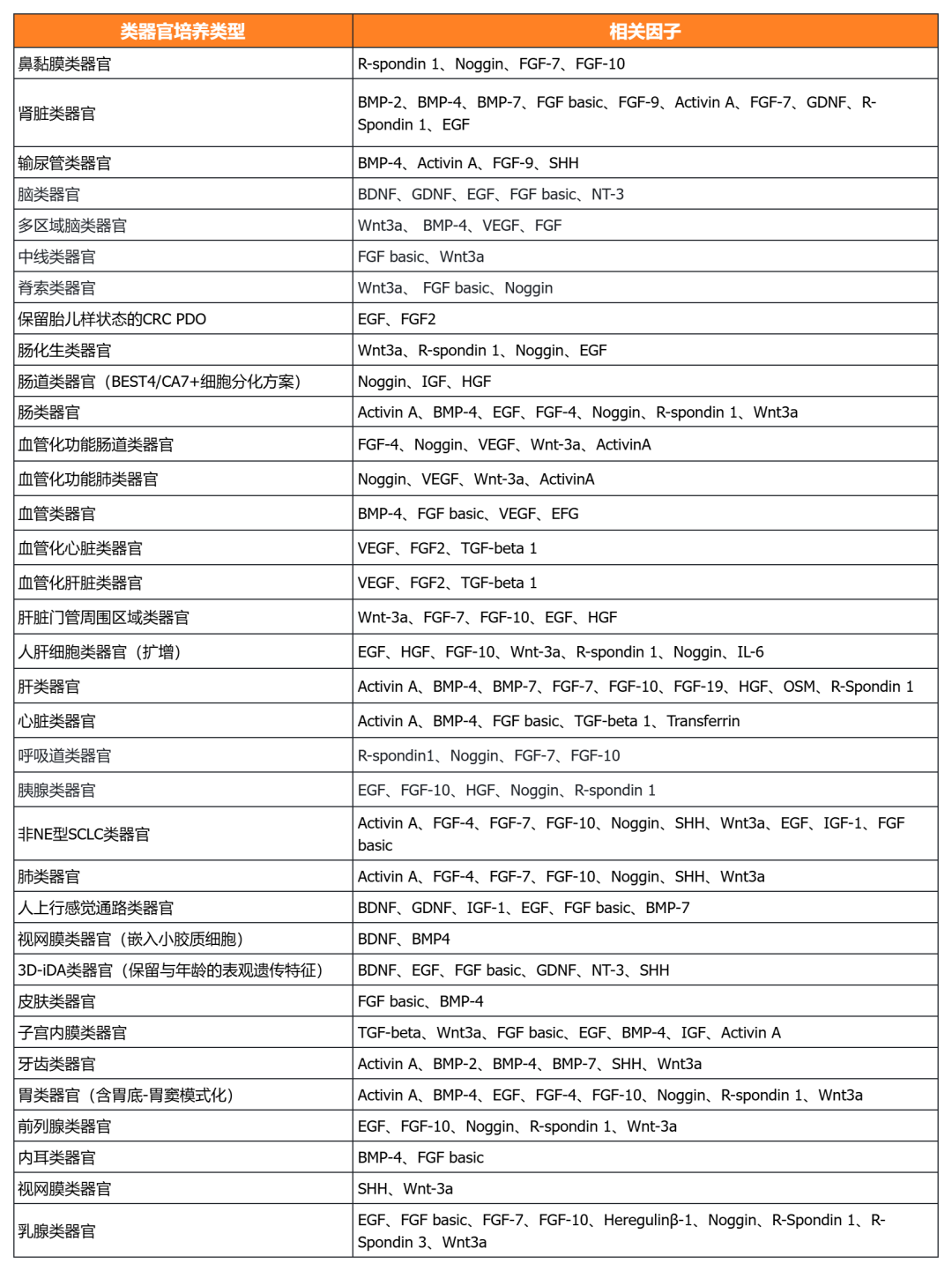
经类器官培养验证的细胞因子
近岸蛋白自主研发生产并经过类器官培养验证的低内毒素Activin A、BMP-4、EGF、FGF-7、FGF-10、FGFb、FGF8b、HGF、IGF1、Noggin、NRG1、R-Spondin 1/3和Wnt3a等细胞因子,已经在人肿瘤类器官如垂体瘤类器官、脑膜瘤类器官、乳腺癌类器官,人正常类器官如ipsc来源的人小肠类器官,以及小鼠正常类器官如小肠类器官、结肠类器官、胃类器官以及胆管类器官等体外模型上进行了验证。
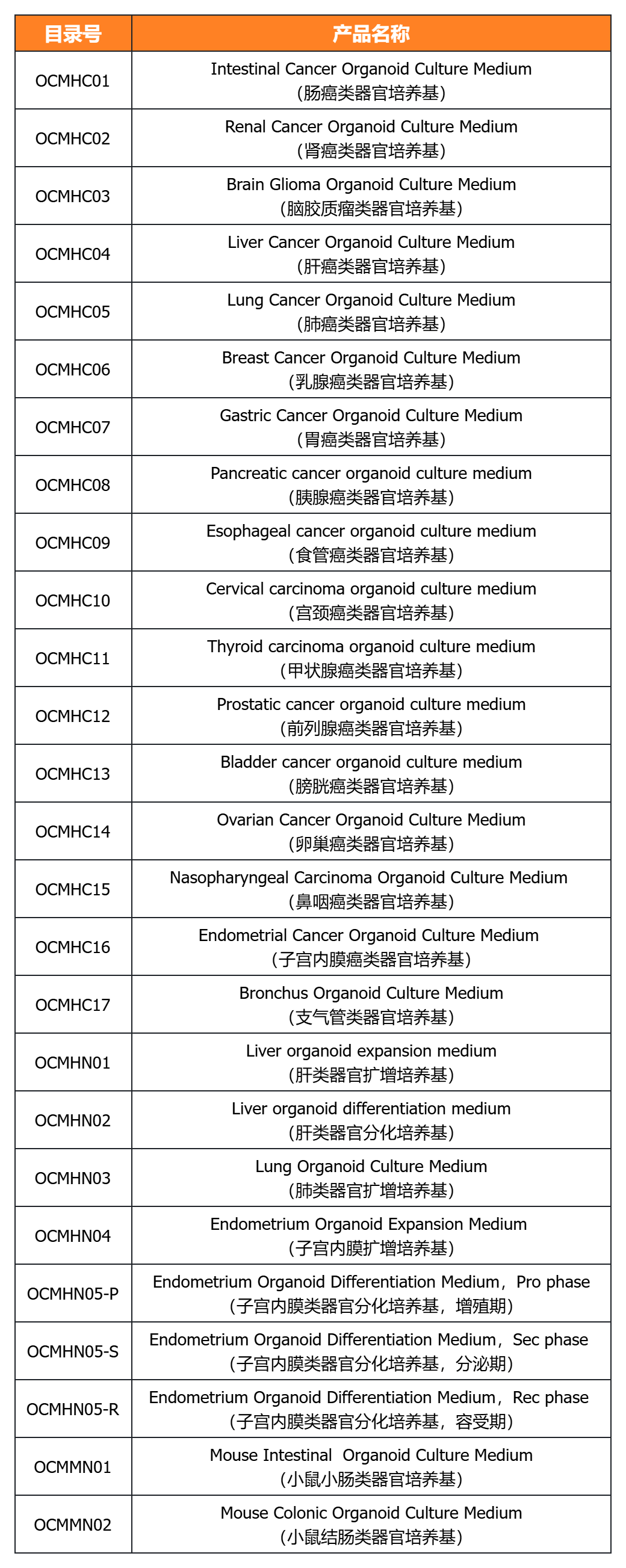
经类器官培养验证的完全培养基
参考资料
1. 【年度重磅】科睿唯安、中国工程院、高等教育出版社联合发布《2024全球工程前沿》
2. Zushin, Peter-James H et al. “FDA Modernization Act 2.0: transitioning beyond animal models with human cells, organoids, and AI/ML-based approaches.” The Journal of clinical investigation vol. 133,21 e175824. 1 Nov. 2023, doi:10.1172/JCI175824
3. Y. Miao et al., “Co-development of mesoderm and endoderm enables organotypic vascularization in lung and gut organoids,”
4. O. J. Abilez et al., “Gastruloids enable modeling of the earliest stages of human cardiac and hepatic vascularization,” Science, vol. 388, no. 6751, p. eadu9375, Jun. 2025, doi: 10.1126/science.adu9375.
5. L. Gong et al., “Rapid generation of functional vascular organoids via simultaneous transcription factor activation of endothelial and mural lineages,” Cell Stem Cell, vol. 32, no. 8, pp. 1200-1217.e6, Aug. 2025, doi: 10.1016/j.stem.2025.05.014.
6. A. Kshirsagar et al., “Multi-Region Brain Organoids Integrating Cerebral, Mid-Hindbrain, and Endothelial Systems,” Adv. Sci. Weinh. Baden-Wurtt. Ger., vol. 12, no. 33, p. e03768, Sep. 2025, doi: 10.1002/advs.202503768.
